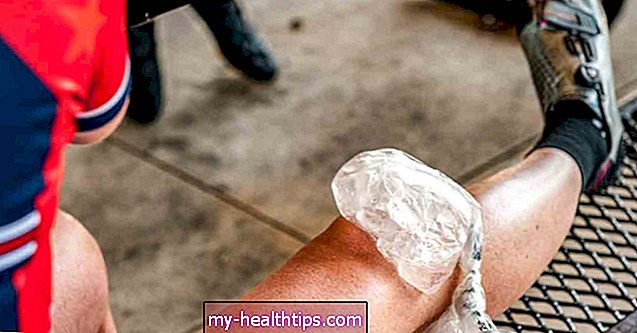
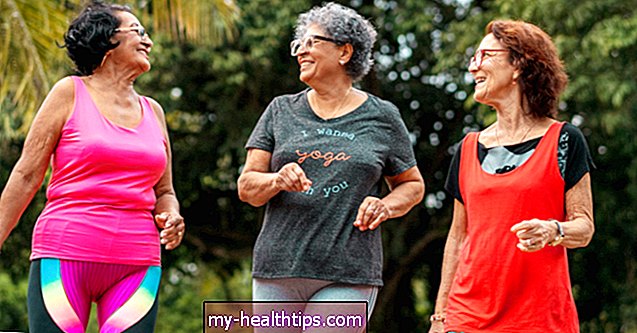Las personas con diabetes que usan una bomba de insulina y un monitor continuo de glucosa (MCG) llevan mucho tiempo soñando con una solución integrada que les permita usar un solo dispositivo en sus cuerpos, en lugar de dos unidades separadas que pinchan su piel en diferentes lugares. Una startup con sede en Oregon bien puede tener la respuesta.
En nuestra reciente Cumbre de Innovación DiabetesMine, la startup Pacific Diabetes Technologies presentó los esfuerzos de la compañía para llevar al mercado un sensor MCG combinado + un equipo de infusión de insulina.
"La razón por la que nos metimos en esto fue la 'carga de dispositivos', donde las personas tienen que usar varios dispositivos y es engorroso", dice el Dr. Ken Ward, un ingeniero de biociencias que ha estado involucrado en la detección de glucosa en compañías como Bayer e iSense antes de cofundar PDT. “A pesar de que la ciencia muestra que estos dispositivos son muy efectivos, muchas personas no usan sus bombas y sensores todo el tiempo. Nuestra creencia es que la 'carga del dispositivo' tiene mucho que ver con eso, por lo que queremos crear un solo dispositivo en el que la cánula y la detección de glucosa sean todo en uno ".
PDT dice que la administración de insulina no interferirá con las lecturas de MCG, habilitado por su sensor hueco con tecnología de "mediador redox" que es diferente a la que usan los fabricantes de MCG existentes en la actualidad.
La compañía tiene un prototipo funcional y actualmente está buscando inversores y socios de investigación, según el CEO y cofundador Robert Cargill.
Algunos recordarán que Medtronic estaba trabajando en una solución integrada similar llamada Minimed Duo hace unos 5 años, pero ese producto nunca se lanzó. PDT ahora está listo para ser el primero en llevar este tipo de dispositivo combinado al mercado.
¿Cómo se verá esto y cómo funcionaría?

El Dr. Ward dice que la TFD tuvo que recurrir a una tecnología novedosa, porque la investigación muestra que si coloca el equipo de infusión de insulina demasiado cerca de los sensores CGM existentes, experimenta un gran aumento en los niveles de glucosa, ¡hasta 800 o 900 mg / dL! Descubrieron esto en estudios con cerdos concluidos hace unos 15 meses en los que los lugares de infusión estaban separados solo unos pocos milímetros.
La causa: conservantes utilizados en la insulina que reaccionan con los sensores CGM tradicionales, lo que significa que tendrían que eliminar los conservantes (no recomendado) o encontrar una forma diferente de realizar la detección CGM.
Mire este video que describe la nueva solución integrada de PDT. Aquí están las especificaciones:
- El primer sensor de MCG "hueco" del mundo que utiliza un tipo diferente de detección de líquido intersticial para que las lecturas de MCG no se vean interferidas por la administración de insulina.
- Un solo dispositivo insertador conectará la unidad combinada al cuerpo, para un uso de 7 días.
- Después de la inserción, colocaría un transmisor (que se asemeja al factor de forma de un Omnipod) en la parte superior para la capacidad CGM.
- Tendrá un período de calentamiento de menos de una hora antes de que se activen las lecturas y alertas de MCG.
- Un transmisor Bluetooth incorporado se comunicará con la tecnología de la nube y el teléfono inteligente. PDT dice que actualmente está considerando la compatibilidad solo con Android primero, y las conexiones de iOS vendrían más tarde.
- PDT dice que busca el estado "no adjunto", lo que significa que los resultados de la MCG podrían usarse para el tratamiento de la diabetes y las decisiones de dosificación, sin necesidad de una punción digital confirmatoria.
- Su primera iteración está diseñada para bombas de insulina con tubos tradicionales, pero también están creando un concepto de bomba de parche. Eso también serviría como una opción para quienes usan bolígrafos de insulina; el usuario insertaba la aguja de la pluma en un puerto superior del transmisor CGM para la administración de insulina en ese lugar sin necesidad de un sitio de inyección adicional.
PDT realizó su primer estudio clínico en humanos en 2018 con 10 pacientes. Los resultados mostraron una precisión de CGM entre 10-14%, que es equivalente o mejor que lo que la mayoría de los fabricantes de CGM vieron en sus productos de primera generación.
Soporte JDRF y cronograma
Hasta la fecha, PDT ha acumulado $ 6 millones en fondos para ayudar a allanar el camino hacia ese primer estudio en humanos el año pasado.
En 2016, la JDRF anunció una asociación con Pacific Diabetes Technologies para crear esta nueva generación de puerto único combinado. Esa subvención de $ 1,14 millones se sumó a los fondos anteriores de los NIH y Helmsley Charitable Trust, lo que preparó a la compañía para su trabajo inicial y futuro de ensayos clínicos.
Desafortunadamente, los plazos se han retrasado un poco. PDT había declarado que esperaba comenzar pruebas fundamentales en 2018, pero eso aún no ha sucedido.
El CEO Cargill nos dice que PDT necesita alrededor de 24 meses a partir de ahora para llegar a una presentación inicial para comenzar sus pruebas fundamentales, asumiendo que pueden encontrar la financiación adecuada para llevar su equipo de I + D a las 18-20 personas necesarias. Él estima que necesitará $ 1.5-3.0 millones por año durante los próximos dos años para que esto suceda. Luego, aproximadamente un año para realizar esos ensayos fundamentales y prepararse para la presentación ante la FDA ... aproximadamente en 2023.
Aún así, los equipos de JDRF y PDT están entusiasmados y esperanzados con las mejoras en la calidad de vida que una solución como esta podría traer a las vidas de las personas que viven con diabetes tipo 1.
"Realmente no ha habido una motivación para las nuevas innovaciones en la tecnología de equipos de infusión, pero todas las investigaciones recientes han vuelto a generar el interés y la emoción", dice el Dr. Ward.






-spread.jpg)